FDA İLAÇ FİRMALARINI UYARDI!
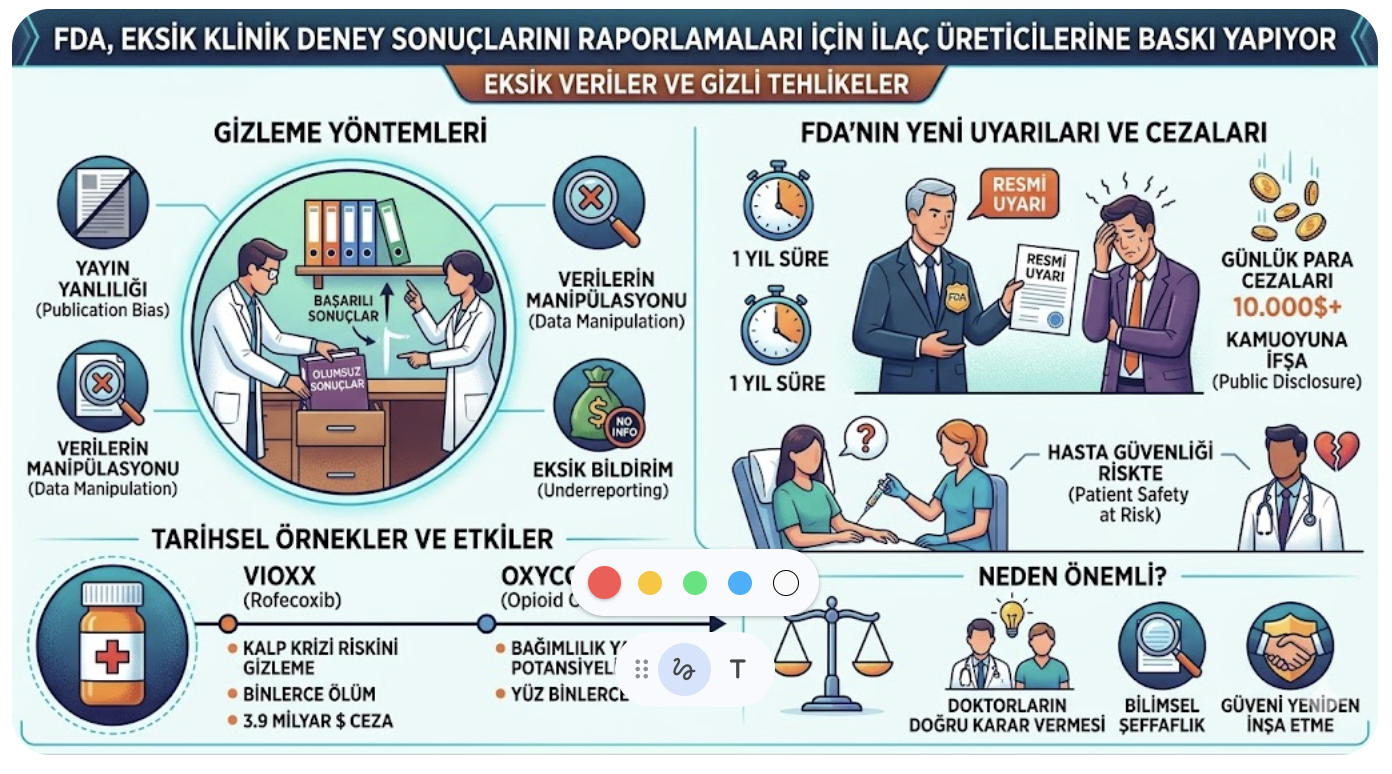
FDA'nın (ABD Gıda ve İlaç Dairesi) klinik araştırma sonuçlarını bildirmeyen vey an etkileri saklayan ilaç firmalarına karşı başlattığı bu hamle, tıbbi şeffaflığı artırmayı ve bilimsel literatürdeki "yayın yanlılığını" (publication bias) engellemeyi amaçlayan geniş kapsamlı bir operasyondur. Nisan 2026 itibarıyla konuyla ilgili öne çıkan detaylar şöyledir:
1. Kapsam ve Uyarılar
FDA, Mart ve Nisan 2026 döneminde 2.200'den fazla tıbbi ürün üreticisi ve araştırmacıya, eksik olan klinik araştırma sonuçlarını kamuoyuna açıklamaları için resmi bildirimlerde bulunmuştur. Bu uyarılar, ClinicalTrials.gov veri tabanında kayıtlı olan ancak yasal süresi dolmasına rağmen sonuçları yüklenmemiş 3.000'den fazla çalışmayı kapsamaktadır.
2. "Yayın Yanlılığı" ve Şeffaflık Sorunu
FDA Başkanı Dr. Marty Makary, şirketlerin genellikle olumsuz sonuçlanan araştırmaları gizlediğini ve bu durumun tıp dünyasında ciddi bilgi boşlukları yarattığını belirtmiştir.
- Başarıların Öne Çıkarılması: Verilerin eksik bildirilmesi, başarısızlıkların gizlenip sadece başarıların gösterilmesine, bu da bir ilacın güvenliği ve etkinliği hakkında çarpık bir algı oluşmasına neden olmaktadır.
- Eksik Veri Oranı: Kurumun iç analizlerine göre, yasal olarak sonuç bildirme zorunluluğu olan çalışmaların yaklaşık %29,6'sının sonuçları halen sisteme yüklenmemiştir.
3. Yasal Zorunluluklar ve Cezalar
ABD yasalarına göre, FDA tarafından düzenlenen ilaç, biyolojik ürün ve tıbbi cihazların (Faz 2'den Faz 4'e kadar olan) araştırmalarının sonuçları, çalışmanın tamamlanmasından itibaren 1 yıl içinde ClinicalTrials.gov adresine yüklenmelidir.
- Uyarı Süreci: FDA önce bir "Ön Bildirim" (Pre-Notice) göndererek tarafları gönüllü düzeltmeye davet etmektedir.
- Maddi Yaptırımlar: Eğer şirket 30 gün içinde düzeltme yapmazsa, günlük 10.000 doları aşan para cezaları ile karşı karşıya kalabilmektedir.
- Kamuoyu İlanı: Uyumsuzluk bildirimleri FDA'nın web sitesinde kalıcı olarak yayınlanmaktadır; bu da şirketler için ciddi bir prestij kaybı anlamına gelmektedir.
Bu girişim, klinisyenlerin ve araştırmacıların bir tedaviye karar verirken sadece başarıları değil, başarısızlıkları ve riskleri de görebilmesini sağlamayı hedefler. Şirketlerin hisse fiyatlarını düşünerek olumsuz verileri saklamasının, hastaların güvenliğini tehlikeye attığı vurgulanmaktadır. Özetle FDA, bilimsel kayıtların tam ve dürüst bir şekilde tutulması için "şeffaflık bir seçenek değil, yasal bir zorunluluktur" mesajını net bir şekilde vermektedir.
4. İlaç Şirketlerinin hileleri?
- Yayın Yanlılığı (Publication Bias): Sadece başarılı olan klinik test sonuçlarını yayınlayıp, başarısız veya yan etkisi çok olan testleri çekmecede saklayarak.
- Veri Madenciliği: İstatistiksel yöntemlerle yan etkileri "anlamsız" veya "başka bir hastalığa bağlı" gibi göstererek.
- Pazarlama Stratejisi: Yan etkileri prospektüsün en kuytu köşelerine koyup, ilacın faydalarını agresif bir şekilde öne çıkararak.
- Bürokrat ve doktorlara rüşvet vererek: Bu bazı firmaların standart yöntemi haline gelmiştir.







