FDA ve TİTCK GERÇEKTEN BAĞIMSIZ MI?
Prof. Dr. F. Cankat Tulunay
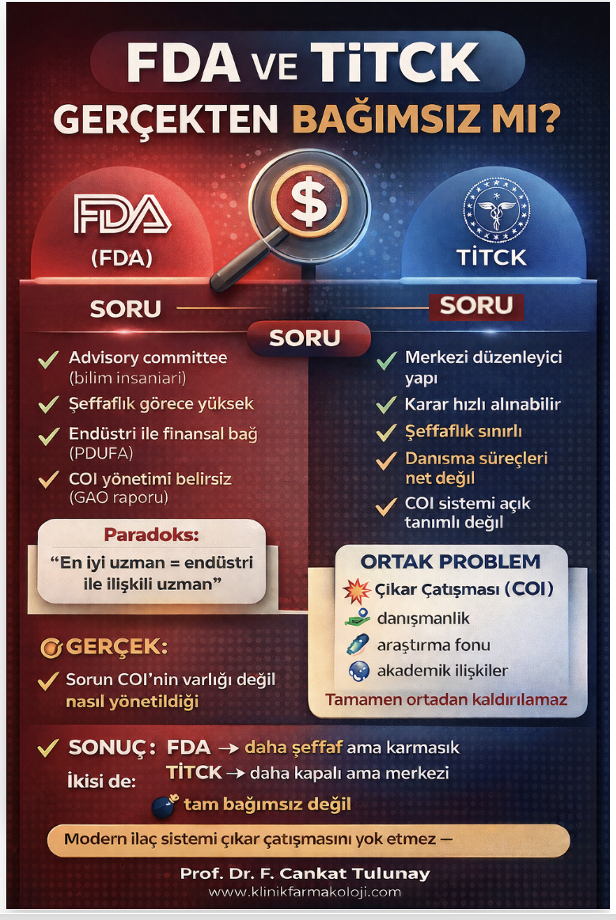
ABD Sayıştayı (Government Accountability Office, GAO) tarafından yayımlanan 2026 tarihli rapor (GAO-26-107877, https://www.gao.gov/assets/gao-26-107877.pdf), ABD ilaç düzenleme kurumu FDA in çıkar çatışmasını (conflict of interest, COI) halen düzenleyemdiğini ortaya koymaktadır. Raporun en temel bulgusu şudur: ABD Gıda ve İlaç Dairesi (FDA), ilaç değerlendirme süreçlerinde görev alan danışma komitesi üyelerinin çıkar çatışmalarını değerlendirmekte, ancak bu değerlendirmeyi hangi kriterlere göre yaptığını açık ve sistematik biçimde kamuya açıklamamaktadır. Kimin neden toplantıya kabul edildiği, kimin neden dışlandığı ve hangi durumlarda istisna (waiver) verildiği net değildir. Daha da önemlisi, bu süreç için yıllardır beklenen resmi rehber 12 yıldır neden tamamlanmamıştır. Sonuç olarak GAO’nun vardığı sonuç FDA in karar mekanizması şeffaf değildir.
Bu bulgu, FDA’nın bağımsızlığı tartışmasını yeniden gündeme getirmektedir. Modern ilaç düzenleme sistemi teoride bilimsel kanıta dayanır. Ancak pratikte bu sistem üç temel aktörün etkileşimi ile çalışır: bilim, regülasyon ve endüstri. FDA bu üçgenin ortasında yer alır. Sorun, bu konumun doğası gereği tarafsızlığın mutlak olamamasıdır. (bu konuda daha detaylı bilgi: http://www.klinikfarmakoloji.com/aci-ilac/fda-and-industry-influence)
Bu yapısal gerilimin en önemli dönüm noktalarından biri 1992 yılında yürürlüğe giren Prescription Drug User Fee Act (PDUFA) olmuştur. Bu yasa ile FDA, ilaç şirketlerinden başvuru değerlendirme ücreti almaya başlamış ve zaman içinde bu gelir, kurum bütçesinin önemli bir kısmını oluşturur hale gelmiştir. Bu durum, ilaç onay süreçlerini hızlandırmış olsa da, regülatör ile endüstri arasında doğrudan bir finansal bağ oluşturmuştur. Bu noktada temel soru ortaya çıkar: denetleyen kurumun, denetlediği sektörden finansal olarak beslenmesi, bağımsızlığı nasıl etkiler?
FDA’nın karar mekanizmasının bir diğer kritik bileşeni advisory committee adı verilen bilimsel danışma kurullarıdır. Bu kurullar, yeni ilaçların değerlendirilmesinde önemli rol oynar. Ancak bu kurullarda yer alan uzmanların büyük bölümü aynı zamanda ilaç endüstrisi ile çeşitli düzeylerde ilişki içindedir. Danışmanlık ücretleri, araştırma fonları ve akademik iş birlikleri bu ilişkinin en yaygın biçimleridir. Bilimsel literatür, finansal ilişkisi olan üyelerin belirli durumlarda firmalar lehine oy verme olasılığının daha yüksek olduğunu göstermektedir. Bu durum bir çelişki yaratır: en yetkin uzmanlar çoğunlukla endüstri ile çalışan kişilerdir. Dolayısıyla çıkar çatışmasını tamamen ortadan kaldırmak, uzmanlığı da ortadan kaldırmak anlamına gelebilir. Modern sistem bu nedenle çıkar çatışmasını yok etmek yerine yönetmeye çalışır. Ancak GAO raporunun ortaya koyduğu temel sorun, bu yönetimin nasıl yapıldığının bilinmemesidir.
Bu yapının sonuçlarını anlamak için geçmişteki büyük ilaç olaylarına bakmak gerekir. Bu olaylar tek tek hatalar değil, sistemin nasıl çalıştığını gösteren örneklerdir.
Vioxx (rofekoksib) vakası bu bağlamda en çarpıcı örneklerden biridir. COX-2 inhibitörü olarak geliştirilen bu ilaç, gastrointestinal yan etkileri azaltma iddiasıyla yaygın şekilde kullanıma girmiştir. Ancak klinik çalışmalar ve post-marketing veriler, ilacın miyokard enfarktüsü ve inme riskini anlamlı şekilde artırdığını göstermiştir. 2004 yılında piyasadan çekilen Vioxx’un, yalnızca ABD’de 88.000–140.000 arasında ciddi kardiyovasküler olaya ve on binlerce ölüme katkıda bulunduğu tahmin edilmektedir. FDA içinde görev yapan bilim insanlarından David Graham, ilacın risklerine erken dönemde dikkat çekmiş, ancak düzenleyici süreçte bu uyarıların yeterince hızlı karşılık bulmadığı görülmüştür. Bu olay, güvenlik sinyallerinin var olmasına rağmen karar süreçlerinin gecikebileceğini göstermiştir.
Bu vakanın daha az tartışılan ancak kritik bir boyutu advisory committee sürecidir. 2005 yılında yapılan FDA danışma kurulu toplantısında, Vioxx ve benzeri COX-2 inhibitörlerinin güvenliği değerlendirilmiştir. Bu toplantıda oy kullanan üyelerin önemli bir kısmının üretici firmalarla finansal ilişkilerinin bulunduğu daha sonra analizlerde ortaya konmuştur. Yapılan yeniden değerlendirmelerde, çıkar çatışması olan üyeler dışlandığında karar dağılımının değişebileceği gösterilmiştir. Bu durum, çıkar çatışmasının kararın yönünü ve zamanlamasını etkileyebileceğini ortaya koymuştur (VIOXX ile ilgili bu sayfalarda daha önce yazılanlar: http://www.klinikfarmakoloji.com/search/node?keys=vioxx)
Benzer bir tartışma Avandia (rosiglitazon) için yaşanmıştır. Bu diyabet ilacı, glisemik kontrol üzerinde etkili olmasına rağmen, 2007 yılında yayımlanan meta-analizler miyokard enfarktüsü riskinde artış olabileceğini göstermiştir. Bu analizlerin başında Cleveland Clinic’ten kardiyolog Steven Nissen yer almakta olup, çalışma ilacın güvenliği konusunda ciddi soru işaretleri doğurmuştur. ABD Senatosu tarafından yürütülen soruşturmalar, üretici firma GlaxoSmithKline’ın bazı risk verilerini yeterince şeffaf biçimde sunmadığını ve veri yorumlarının tartışmalı olduğunu ortaya koymuştur. Advisory committee sürecinde yer alan bazı üyelerin firma ile finansal ilişkilerinin bulunması, bu tartışmayı daha da derinleştirmiştir. Sonuçta ilaç ABD’de ciddi kısıtlamalara tabi tutulmuş, Avrupa’da ise bir dönem piyasadan çekilmiştir. Avandia vakası, klinik fayda ile kardiyovasküler risk arasındaki dengenin nasıl yorumlanacağı konusunda bilimsel ve düzenleyici çatışmayı açık biçimde ortaya koymuştur. (AVANDİA ile ilgili bu sayfalarda daha önce yazılanlar: http://www.klinikfarmakoloji.com/search/node?keys=avandia)
Opioid krizi ise çıkar çatışmasının halk sağlığı üzerindeki en dramatik etkilerinden birini temsil eder. OxyContin (oksikodon), Purdue Pharma tarafından 1990’ların ortasında piyasaya sunulurken bağımlılık riskinin düşük olduğu yönünde agresif bir pazarlama stratejisi ile tanıtılmıştır. Ancak gerçek klinik kullanımda bu riskin ciddi biçimde hafife alındığı ortaya çıkmıştır. ABD’de opioidler ile ilişkili ölümlerin sayısı 1999’dan bu yana 500.000’in üzerine çıkmış, yalnızca son yıllarda yıllık ölüm sayısı 80.000’in üzerine ulaşmıştır. Purdue Pharma ve Sackler ailesinin rolü, bu krizin yalnızca farmakolojik değil aynı zamanda kurumsal ve ekonomik bir yapıdan kaynaklandığını göstermiştir. Şirket 2007 yılında suçunu kabul etmiş, 2020 sonrasında ise milyarlarca dolarlık tazminat anlaşmaları gündeme gelmiştir. Bu süreçte yalnızca doğrudan pazarlama değil, hekimlere yönelik eğitim programları, danışmanlık ödemeleri ve akademik ilişkiler üzerinden kurulan geniş finansal ağın, opioidlerin risk algısını sistematik biçimde değiştirdiği görülmüştür (bu konuda bu sayfalarda daha önce yazılanlar: http://www.klinikfarmakoloji.com/search/node?keys=oxycontin)
Daha yakın dönemde Aducanumab örneği, düzenleyici kararların bilimsel danışma süreçlerinden nasıl ayrışabileceğini göstermiştir. Alzheimer hastalığı için Biogen tarafından geliştirilen bu ilaç, klinik çalışmalarında bilişsel fayda açısından tutarsız ve sınırlı sonuçlar göstermesine rağmen 2021 yılında FDA tarafından hızlandırılmış onay almıştır. FDA danışma komitesindeki üyelerin büyük çoğunluğu ilacın onaylanmasına karşı oy kullanmış, buna rağmen FDA onay kararı vermiştir. Bu kararın ardından Harvard’dan Aaron Kesselheim ve Washington University’den Joel Perlmutter dahil olmak üzere en az üç danışma kurulu üyesi istifa etmiştir. Bu durum modern FDA tarihinde nadir görülen bir kurumsal kırılma olarak değerlendirilmiştir. Ayrıca FDA ile Biogen arasında onay sürecinde olağan dışı yakın etkileşim olduğu yönünde eleştiriler gündeme gelmiştir. İlacın yıllık maliyetinin başlangıçta 56.000 dolar olarak belirlenmesi ve klinik faydanın belirsizliği, bu kararın ekonomik ve bilimsel boyutunu daha da tartışmalı hale getirmiştir (bu konuda bu sayfalarda daha önce yazılanlar: http://www.klinikfarmakoloji.com/search/node?keys=aducanumab)
Bu örnekler birlikte değerlendirildiğinde verilerin nasıl yorumlandığı, hangi hızda değerlendirildiği ve karar süreçlerine nasıl yansıtıldığı ortaya çıkar. Çıkar çatışması doğrudan yanlış karar üretmekten çok, kararların yönünü, tonunu ve zamanlamasını etkileyen bir faktör olarak ortaya çıkar. Riskler daha geç kabul edilir, faydalar daha erken vurgulanır ve belirsizlikler çoğu zaman iyimser yorumlanır ve ilaç firmasının çıkarına kararlar verilir.
Bu olaylar, çıkar çatışmasının bireysel bir problem olmaktan çok yapısal bir özellik olduğunu göstermektedir. Endüstri tarafında ise rüşvet ve yolsuzluk vakaları daha açık biçimde belgelenmiştir. GlaxoSmithKline’ın Çin’de doktorlara sistematik ödeme yapması, Teva ve Novartis gibi firmaların farklı ülkelerde kamu görevlileri veya hekimlerle finansal ilişkileri nedeniyle büyük cezalar alması, bu sistemin ekonomik boyutunu ortaya koymaktadır. FDA içinde doğrudan rüşvet vakaları nadir olsa da, endüstri ile akademi ve klinik pratik arasındaki finansal ağ son derece yoğundur.
Türkiye açısından bakıldığında TİTCK yapısı farklı olmakla birlikte benzer tartışmaların mevcut olduğu görülmektedir. Türkiye’de ilaç ruhsatlandırma ve değerlendirme süreçleri Türkiye İlaç ve Tıbbi Cihaz Kurumu (TİTCK) tarafından yürütülmekte ve bu süreçte çeşitli bilimsel danışma kurulları rol almaktadır. Ancak bu kurulların nasıl oluşturulduğu, üyelerin hangi objektif kriterlere göre seçildiği ve karar süreçlerinin ne ölçüde bağımsız olduğu konusunda kamuya açık ve sistematik bir şeffaflık bulunmamaktadır.
Danışma kurulu üyelerinin seçiminde liyakat, çıkar çatışması değerlendirmesi ve görev süresi gibi kriterlerin açık ve standartlaştırılmış biçimde tanımlanmamış olması, karar süreçlerinin kurumsal bağımsızlığı konusunda soru işaretleri doğurmaktadır. Ayrıca Danışma kurulu üyelerinin kurum başkanı veya bakanlık üst yönetimi tarafından tavsiye edilen kişilerden oluşması ve idarenin uygun görmediği kararları veren üyelerin değiştirlmesi de tartışma konusudur.
Bu yapı içinde ortaya çıkan temel risk, belirli kararların kurumsal tercihleri yansıttığı algısının oluşmasıdır. Danışma kurullarının sürekliliği, üyelerin görevden alınma veya değiştirilme koşulları ve farklı görüşlerin karar süreçlerine ne ölçüde yansıdığı konularında yeterli şeffaflık olmaması, bilimsel bağımsızlık tartışmalarını kaçınılmaz hale getirmektedir.
Bu nedenle Türkiye’de asıl tartışılması gereken konu, çıkar çatışmasının varlığı değil, bilimsel danışma süreçlerinin nasıl yapılandırıldığı, ne ölçüde bağımsız olduğu ve kamu tarafından ne kadar denetlenebilir olduğudur.
Sonuç olarak modern ilaç sistemi, çıkar çatışmasını ortadan kaldıran bir sistem değildir; onu yöneten bir sistemdir. Ancak GAO raporunun gösterdiği gibi, bu yönetim süreci yeterince şeffaf değildir. Bu nedenle tartışılması gereken temel konu, çıkar çatışmasının varlığı değil, nasıl yönetildiği ve bu yönetimin kamu tarafından ne kadar denetlenebildiğidir.
Sonuç olarak: FDA veya TİTCK tamamen bağımsız kurumlar değildir. Sorun bireysel hatalardan çok systemin yapısındadır ve çıkar çatışması da bu systemin bir parçasıdır. Çıkar çatışması sistematik olarak halk sağlığını bozar.







