ZOMBİ KLİNİK ARAŞTIRMALAR VE SAHTE İLAÇ ARAŞTIRMALARI
Prof. Dr. F. Cankat Tulunay, The European Association for Clinical Pharmacology and Therapeutics (EACPT) onursal başkanı
"Pivotal clinical trial" (önemli veya kritik klinik deneme) terimi, bir ilaç, tedavi ya da tıbbi cihazın etkinliğini ve güvenliğini belirlemek için yapılan, genellikle onay almak amacıyla yapılan, büyük ve kapsamlı klinik denemelerdir. Bu denemeler, düzenleyici otoriteler (örneğin FDA, EMA) tarafından ilaçların veya tedavilerin piyasaya sürülüp sürülmemesine karar verilmesinde esas alınan ana verileri sağlar. Pivotal bir çalışma genellikle çok yıllı bir klinik araştırma sürecindeki Faz III klinik çalışmadır. Bu çalışma, bir tedavinin –örneğin bir ilaç adayı, tıbbi cihaz veya klinik tanı prosedürü– güvenliğini ve etkinliğini göstermek ve doğrulamak amacıyla gerçekleştirilir ve yaygın yan etkilerin görülme sıklığını tahmin etmeyi amaçlar ve yüzlerce- binlerce denekle yürütülür (1)
2017 yılında Amerika Birleşik Devletleri’nde, tüm klinik endikasyonlar için bir pivotal çalışmanın medyan maliyeti 19 milyon ABD doları idi. Katılımcı sayısı arttığında, aktif ilaç karşılaştırıcılar kullanıldığında (deneme ilacının özelliklerini daha iyi anlamak amacıyla), ya da yerine birincil klinik sonuçlar ölçüldüğünde (dolaylı, ikincil-surrogate sonuçlar yerine), çalışmanın maliyeti artmaktaydı (2).
2019’un sonlarında, ABD Adalet Bakanlığı’nın (“DOJ”) Tüketici Koruma Birimi (“CPB”) Direktörü Gustav Eyler, yeni ilaçlar ve tıbbi cihazlarla ilgili klinik araştırma çalışmalarında sahte verilerin kullanılması konusunu “önemli bir endişe kaynağı” olarak nitelendirdi. Klinik araştırma sahtekârlığı vakaları genellikle FDA’nın Ceza Soruşturmaları Ofisi tarafından başlatılır ve çoğunlukla DOJ’un CPB veya Sağlık Dolandırıcılığı Birimi tarafından dava edilir. Bu soruşturmalar karmaşıktır ve sonuçlanması genellikle yıllar alır.
Çok büyük ilaç firmaları da sıklıkla sahte araştırmalar ile ruhsat başvurusunda bulunabilir. Örneğin, İlaç devi Pfizer tarafından yürütülen ilaç denemelerine dair kamuya açık ve şirket içi tanımlar karşılaştırıldığında, çalışmaya katılan kişi sayısında değişiklikler ve protokol ile analizlerin tanımlarında tutarsızlıklar gibi çelişkiler tespit edilmiştir. John Hopkins Bloomberg sHalk Sağlığı bölümü direktörü Kay Dickersin ve arkadaşları, bir dava dolayısı ile Pfizer’in iç yazışmalarına erişti. Araştırmacılar, bu iç belgeleri Pfizer’ın epilepsi ilacı gabapentin’in (marka adı: Neurontin) farklı rahatsızlıklar için etkinliğini test eden randomize klinik çalışmalara ilişkin 10 hakemli dergi yayınıyla karşılaştırdılar ve sonuçların yayımlanan çalışmaların yanlı ve yanıltıcı olduğunu gösterdiğini, standart protokollere uyulmuş gibi görünmelerine rağmen durumun böyle olmadığını tesbit ettiler.
Araştırmacılar, incelenen on endüstri destekli çalışmadan üçünde, randomize edilen katılımcı sayısı açısından iç araştırma raporu ile ana yayın arasında farklılıklar olduğunu buldu. Ayrıca, on çalışmadan altısında araştırmacılar, iç raporda birincil sonucun tanımlanmamış olması ya da analiz türünün belirtilmemesi nedeniyle, etkinlik açısından analiz edilen katılımcı sayısını karşılaştıramadı. Bir çalışmada, katılımcıların %40’ına ait veriler yayımlanan sonuçlara dahil edilmemişti. Genel olarak, araştırmacılar protokoller, istatistiksel analiz planları ve yayınlarda yedi farklı etkinlik analiz türünün tanımlandığını tespit etti. Bu analiz türlerinden biri olan "niyetlenilen tedavi" (intention-to-treat) analizi için protokolde veya yayında altı farklı tanım kullanıldığı görüldü. Bu durum, analiz edilen hasta sayıları konusunda iç raporlar ile yayımlanmış makaleler arasında önemli farklara yol açtı. Pfizer, 2010 yılında bir davayı kaybetti ve şirketin Neurontin’i migren ve bipolar bozukluk tedavisinde yasa dışı tanıtımı nedeniyle federal organize suç yasalarını ihlal ettiğine karar verildi. Şirket, 142 milyon dolar tazminat ödemeye mahkûm edildi. Pfizer daha önce, 2004 yılında da Neurontin’i onaylanmamış kullanımlar için pazarladığı gerekçesiyle 430 milyon dolar sivil ceza ve cezaî yaptırımlar ödeyerek bir davayı sonuçlandırmıştı. (3)
Bilimsel araştırmalarda etik ihlaller çok çeşitli biçimlerde ortaya çıkabilir. Bu ihlallerin çoğu, bilimsel üretim sürecinin farklı aşamalarında — veri toplama, analiz, raporlama, yayınlama — meydana gelir. En yaygın görülen etik dışı uygulamalar arasında aşağıdaki kategoriler öne çıkmaktadır:
- Veri uydurma (fabrication): Hiç yapılmamış bir araştırmanın veya deneyin yapılmış gibi gösterilmesi; gerçek olmayan verilerin üretilerek sunulması.
- Veri çarpıtma (falsification): Gerçek verilere müdahale edilerek değiştirilmesi, bazı verilerin gizlenmesi veya analizlerin kasıtlı olarak yanıltıcı şekilde yapılması.
- İntihal (plagiarism): Başka bir araştırmacının fikir, metin, veri veya görsel materyalini kaynak göstermeksizin kullanmak.
- Yayın etiği ihlalleri: Aynı çalışmayı birden fazla yerde yayımlamak (duplikasyon), makalede katkısı olmayan kişileri yazar olarak göstermek veya katkısı olanları dışlamak.
- Etik kurul izni olmaksızın insan/denek çalışmaları yapmak.
- Yayın sürecinde manipülasyon: Sahte hakemler kullanmak, kendi kendine atıf veya atıf çeteleri yoluyla akademik etkiyi yapay olarak artırmak.
Ioannidis JPA yaptığı araştırmada, 1 Ocak 1986 ile 4 Aralık 2015 tarihleri arasında, PubMed’de 266.782 "sistematik derleme" ve 58.611 "meta-analiz" yayinlanmış. Aynı konuda yapılan meta-analizlerin sayısı bazen 20’yi aşmaktadır. Bazı alanlarda yoğun şekilde meta-analiz üretilmektedir; örneğin, 2007 ile 2014 yılları arasında depresyon için antidepresanlarla ilgili 185 meta-analiz yayınlanmıştır. Bu meta-analizlerin çoğu, ya doğrudan endüstri çalışanları tarafından yapılmakta ya da endüstriyle bağlantılı yazarlar tarafından kaleme alınmakta ve sonuçlar genellikle sponsorların çıkarlarıyla uyumlu olmaktadır. Çin kaynaklı meta-analizlerin en yoğun olduğu alanlardan biri genetik ilişkilerdir (2014'te küresel üretimin %63'ü); ancak bu alandaki sonuçların neredeyse tamamı yanıltıcıdır. Ayrıca, kanıt sentezi alanında çalışan birçok taşeron şirket, endüstriden meta-analiz üretimi için sözleşmeli işler almakta ve bunların bir kısmı muhtemelen hiç yayımlanmamaktadır. Yayınlanan meta-analizlerin pek çoğunda da ciddi hatalar bulunmaktadır. Geri kalan çalışmaların çoğu ise karar vermeye yetecek düzeyde güçlü kanıt sunmaktan uzaktır. Sistematik derleme ve meta-analiz üretimi epidemik boyutlara ulaşmıştır. Büyük olasılıkla yayımlanan sistematik derleme ve meta-analizlerin çok büyük bir kısmı gereksiz, yanıltıcı ve/veya çıkar çatışmasına sahip niteliktedir (4)
California Üniversitesinde yapılan bir araştırmada, önde gelen tıbbi dergilerde yayımlanan yeni tedavilerin çoğu randomize klinik deneylerinin, kullanılan istatistiklerin sonuçları yanıltıcı olabileceği iddiasında bulundular.1989 ile 1998 yılları arasında, Annals of Internal Medicine, BMJ, JAMA, Lancet ve New England Journal of Medicine gibi beş büyük tıbbi dergide yayımlanan 359 yeni tedaviye yönelik randomize klinik denemeyi incelediler. Araştırmacılar, denemelerin çoğunun sonuçları, aktif tedavi ile plasebo veya karşılaştırmalı tedavi arasındaki son noktalarındaki (end point) yüzde farkını, yani göreceli risk azalmasının (relative risk reduction) temel alarak sunduğunu buldular. Çalışma, incelenen makalelerin yalnızca 18'inin mutlak risk azalmasını (absolute risk reduction), tedavi ile plasebo sonuçları arasındaki gerçek farkı, ele aldığını gösterdi. 359 denemenin sadece sekizi, tedavi edilmesi gereken hasta sayısını (number needed to treat) rapor etti. Bir ilaç değerlendirilirken, en azından mutlak risk azalmasının gösterilmesi gereklidir. Göreli risk azalması, mutlak risk azalması aslında çok küçük olsa bile oldukça büyük görünebilir." Örneğin, bir hastalık her milyon kişiden iki kişiyi öldürüyorsa, ölüm oranını bir milyonda bir kişiye indiren bir ilaç, %50'lik bir göreli risk azalması sağlar ki bu da büyük bir fayda gibi görünür. Ancak, mutlak risk azalması yalnızca bir milyonda bir olacaktır (5)
Carlisle JB, bazı araştırmaların sahte veriler içerdiğinden endişe duyarak, Şubat 2017 ile Mart 2020 arasında Anaesthesia dergisine gönderilen randomize kontrollü çalışmaların temel özet verilerini analiz etti. Verileri sahte olan çalışmaları, eğer çalışmanın ölümcül bir kusuru olduğunu düşünüyorsa, “zombi” olarak sınıflandırdı. 526 gönderilen çalışmayı analiz edildiğinde: 73’ünde (%14) sahte veri vardı ve 43’ünü (%8) zombi olarak sınıflandırıldı. Bireysel hasta verileri, sahte verilerin tespit edilmesini ve çalışmaların zombi olarak sınıflandırılmasını, bireysel hasta verisi olmayan çalışmalara kıyasla artırdı: bireysel hasta verisi olanlarda 153 çalışmadan %44ü sahte iken, olmayanlarda 373 çalışmadan %2si sahteydi; aynı şekilde, 153 çalışmadan %26 zombi iken, 373 çalışmadan yalnızca %1 zombiydi. Bireysel hasta verisinin analizi, sahte verilerle olasılık oranı (%95 güvenilirlik aralığı 47 (17–144) ve zombi çalışmalarla olasılık oranı (%95 güvenilirlik aralığı 79 (19–384) bağımsız olarak ilişkiliydi. Beş ülkenin yazarları, gönderilen sahte çalışmaların çoğunluğunu oluşturdu: Gönderilen randomize kontrollü çalışmaların bireysel hasta verilerinin incelenmesi, %44 oranında sahte veri ortaya çıkardı. Turner ve arkadaşları antidepressanların FDA’e ruhsat müracaatı sırasında verilen 74 araştırmadan 23 ünün (%31) yayınlanmadığını, yayınlanan çalışmalarda mediyan hasta sayısının 153, yayınlanmayan çalışmalarda 146 olduğunu tesbit etmişler. FDA 74 çalışmanın 38 ini (%51) pozitif, 36 çalışmayı negative (24 çalışma), veya sorgulanır (12) bulmuş ve negative 36 çalışmadan 3’ü yayınlanmış diğerleri yayınlanmamıştır. Yayınlanan 51 çalışmanın 48’ı pozitif sonuç olanlardır (%94). Çalışmalara toplam 12.564 hasta katılmıştır. Çalışmaya katılan 3449 hastanın (%27) sonuçları açıklanmamıştır. Yayınlanan 1843 (%15) hastanın ise SONUÇLARI İLE OYNANMIŞTIR (6,7) 2019'un başından itibaren Anaesthesia Dergisi, en fazla sayıda makale gönderen ülkelerden (Mısır; Çin anakarası; Hindistan; İran; Japonya; Güney Kore; ve Türkiye)) yazarlar tarafından klinik çalışmalar sunulur sunulmaz bireysel hasta verilerini talep etti. Araştırma sırasında Anesthesia Dergisinde Türkiyede yapılmış 8 zombi araştırma tesbit edildi. Carlisle JB, bazı araştırmaların sahte veriler içerdiğinden endişe duyarak, Şubat 2017 ile Mart 2020 arasında Anaesthesia dergisine gönderilen randomize kontrollü çalışmaların temel özet verilerini analiz etti. Verileri sahte olan çalışmaları, eğer çalışmanın ölümcül bir kusuru olduğunu düşünüyorsa, “zombi” olarak sınıflandırdı. 526 gönderilen çalışmayı analiz edildiğinde: 73’ünde (%14) sahte veri vardı ve 43’ünü (%8) zombi olarak sınıflandırıldı. Bireysel hasta verileri, sahte verilerin tespit edilmesini ve çalışmaların zombi olarak sınıflandırılmasını, bireysel hasta verisi olmayan çalışmalara kıyasla artırdı: bireysel hasta verisi olanlarda 153 çalışmadan %44ü sahte iken, olmayanlarda 373 çalışmadan %2si sahteydi; aynı şekilde, 153 çalışmadan %26 zombi iken, 373 çalışmadan yalnızca %1 zombiydi. Bireysel hasta verisinin analizi, sahte verilerle olasılık oranı (%95 güvenilirlik aralığı 47 (17–144) ve zombi çalışmalarla olasılık oranı (%95 güvenilirlik aralığı 79 (19–384) bağımsız olarak ilişkiliydi. Beş ülkenin yazarları, gönderilen sahte çalışmaların çoğunluğunu oluşturdu: Gönderilen randomize kontrollü çalışmaların bireysel hasta verilerinin incelenmesi, %44 oranında sahte veri ortaya çıkardı (8).Tıp ve bilimsel araştırmalar, insan sağlığını geliştirme misyonuyla yürütülmesi gereken en güvenilir alanlar arasında yer alır. Ancak son yıllarda, klinik araştırmaların giderek artan bir kısmı “zombi çalışmalar” (ya da “hayalet araştırmalar”) olarak adlandırılan bilimsel açıdan ölü ama hala dolaşımda olan yayınlarla dolmaya başladı. Bu çalışmalar ya asla gerçekleştirilmemiştir ya da sahte verilerle, etik dışı yöntemlerle ya da şirket çıkarları doğrultusunda manipüle edilerek yayımlanmıştır. Sonuç: tıbbi kararların, kılavuzların ve kamu politikalarının hatalı veriler üzerine inşa edilmesi.“Zombi çalışma” terimi, bilimsel literatürde teknik olarak varlığını sürdüren fakat bilimsel olarak “ölü” olan araştırmaları tanımlar. Zombi çalışmaların ortaya çıkmasında kilit faktörlerden biri de etik kurulların ve yayın süreçlerinin yeterince denetlenmemesidir. Pek çok ülkede, özellikle de düşük ve orta gelirli ülkelerde, etik kurul onayları “formaliteden” ibaret hale gelmiştir. Bazı üniversitelerde etik kurullar, üniversitenin bir rektörlük birimi gibi çalışmakta ve araştırmacılarla çıkar çatışması yaşamaktadır. Benzer şekilde, predatör (yağmacı) akademik dergilerde yayınlanan “sözde bilimsel” makaleler, hakemlik sürecinden geçmeden yayınlanmakta ve bu dergilerde yayımlanan sahte çalışmalar, daha sonra ciddi akademik çalışmalarda kaynak gösterilebilmektedir. Bilimsel literatürde yayımlanmış her makalenin doğru olduğu varsayımı artık geçerliliğini yitirmiştir. Zombi klinik araştırmalar, sahte ilaç çalışmaları ve bilimsel etik dışılık; tıp, biyoloji ve hatta psikoloji gibi alanlarda güven krizine neden olmaktadır. Gerçek bilimi savunmak, yalnızca araştırmacıların değil, bilim gazetecilerinin, editörlerin ve kamuoyunun da sorumluluğudur. Bunlar çoğunlukla şunları içerir: Gerçekleştirilmemiş ama yayınlanmış klinik deneyler, Sahte ya da uydurma verilerle yazılmış makaleler ve Geri çekilmiş ama alıntılanmaya devam eden yayınlar. Zombi çalışmalar yalnızca bireysel akademik dürüstlük meselesi değildir. Daha büyük sistematik etkiler yaratırlar:
- Sistematik derlemelere girerler: Bu çalışmalar Cochrane gibi saygın kurumların analizlerine bile sızabilir.
- Klinik rehberleri etkilerler: FDA veya EMA onaylarında bu veriler referans alınabilir.
- Yatırımları yönlendirirler: Kamu fonları, sahte başarı gösteren alanlara kaydırılabilir.
- Hastalara zarar verirler: Hatalı ilaç kullanımı ve tedavi seçimlerine neden olabilirler.
Bilimsel literatürdeki sahtekarlıkların en büyüklerinden birisi Tokyo Taho Üniversitesinden anesteziyolog Yoshitaka Fujii’ye aittir. Fujii’nin son on senede yazdığı 200 makalenin 172 tanesi sahte çıktı ve üniversiteden kovuldu. Sahtekarlık yanlız Japonyada değildi. 2009 Yılında Boston Tufts üniversitesinden Scott Reuben’in 21 yayını veri uydurduğu için geri çekildi. Reubenin bu makalelerinin çoğu Pfizer’den Celecoxib ve Lyrica için para alarak yaptığı ortaya çıktı ve Reuben üniversiteden kovuldu (hikayenin tamımını merak edenler için (9) linkinden okuyabilirler). Benzer birolay da Almanyada Ludwigshafen hastanesinden Joachim Boldt’un yayınlarında görüldü ve 90 yayını 11 dergiden çıkartıldı.2022 yılında yayımlanan bir çalışmaya göre, Türkiye’den araştırmacılar tarafından yazılmış 86 biyomedikal makale bilimsel dergilerden geri çekilmiştir. Geri çekilme nedenleri arasında en yaygın olanlar: İntihal (23 makale), yinelenen yayın (22 makale), Hatalar (17 makale) olarak belirtilmiş (10). 2021 yılında yapılan başka bir araştırma ise, farklı bilim alanlarında Türk yazarlar tarafından yazılmış 147 makalenin geri çekildiğini göstermektedir. Bu çalışmada 1083 yayın taranmış, bunlardan 667 tanesi tekrarlanan (dublicate) ve 269 u da çalışma ile alakasız bulunmuştur. Geri çekilme nedenleri arasında en yaygın olanı yinelenen yayın (%34) bulunmuş ve geri çekilme kararlarının çoğu baş editör tarafından verilmiştir (%42,9). Yayınların çoğu tıp bilimleri alanında (%63,3) yer almaktadır. Bu alanlar içinde en çok geri çekilme cerrahi ve ilgili branşlarda (n = 44) olmuştur. En fazla geri çekilme Hacettepe Üniversitesi yayınlarında olmuştur (11). Geri çekmelerin en önemli sebeplerinden birisi akademik yükselmeler için yayın sayısı kriteridir. Özellikle taşra üniversitelerinde ve belli cemaat mensupları arasında ‘’İMECE’’ yayın Türkiyede çok yaygındır ve maalesef bu yayınlar jüriler tarafından özellikle yandaşlık ve nepotism sebebi ile kabul edilmektedir. Bir sayfalık, tek bir olgu sunumu yayınında çeşitli illerden 8 kişinin ismini bulabilirsiniz. Yayın kalitesindeki diğer bir sahtekarlık ise bazı grupların kendi dergilerini çıkartmaları ve kendi içinden yayınlarını yapmalarıdır. Hatta Türkiyede sahibi, baş editörü ve yazarı ayni kişi olan dergi bile bulmak mümkündür. Bazı kurumların (üniversite, fakülte, hastane gibi) kendi yayınları da farklı değildir.
Tıpta bilim dışı dini referansları kullanan, ve bir Türk üniversinden yayınlanan bir çok makale yayından kaldırılmıştır, bazı örnekler (12):
- “Multipl Sklerozlu Hastalarda Din, Maneviyat ve Manevi Bakımın Önemi’’ published on May 22, 2023 in Journal of Pediatric Neurology
- ‘’Tesettür Ergenlik Çağındaki Kızları ve Kadınları Cinsel Tacizden Koruyor,” published on May 26, 2023 in Journal of Pediatric Neurology
- “İslam Psikolojisi: Herbert George Wells'ten (1866-1946) Tarihsel Notlar,” published on Nov. 16, 2022 in Journal of Pediatric Neurology
- “Anne-Baba İlişkisinde Evlilik ve Evlilik Sadakati: Dini Perspektiften Bir Bakış," published on May 4, 2023 in Journal of Child Science
- "Yenidoğan Yoğun Bakım Ünitesinde Dini Başa Çıkmanın Rolü,” published on May 4, 2023 in Journal of Child Science
- “Ruqyah ve Kanserli Hastalar Arasında Kullanımı,” published on March 20, 2023 in Journal of Child Science
- “Neonatal Hipoglisemi: Oral Dekstroz Jel ve Tahneek Uygulaması,” published in June 2023 in the Journal of Pediatric Epilepsy
İstanbul Medeniyet üniversitesinden COVİD 19 tedavisi ile ilgili bir makale hastaların onayı alınmadan, etik kurallara aykırı olarak yapıldığı için deriden çıkartılmış (13)
Yanıltıcı veya uygunsuz klinik araştırmalardaki diğer bir sorun da yalancı ve sahtekar deneklerle yapılan araştırmalardır. Aldatıcı deneğin davranışı, araştırma bulgularının bütünlüğü için bir tehdit oluşturur. Bu denekler, profesyonel kobaylar, sübversif araştırma denekleri, profesyonel denekler, mükerrer denekler olarak tanımlanmışlardır. Bunlar genellikle araştırmalardan para kazanan br nevi profesyonellerdir ve bunların verdikleri bilgilere güvenilemez. Bazıları ayni anda 2 araştırmaya katılabilirler (Afrikada HIV proflaksi çalışmasında deneklerin %34’ü başka çalışmalara da katılmıştır). Özellikle uzun süreli ve hastane dışında yapılan araştırmalarda denekler ilaçları muntazam kullanmadığı gibi sonuçları da uydururlar (14).
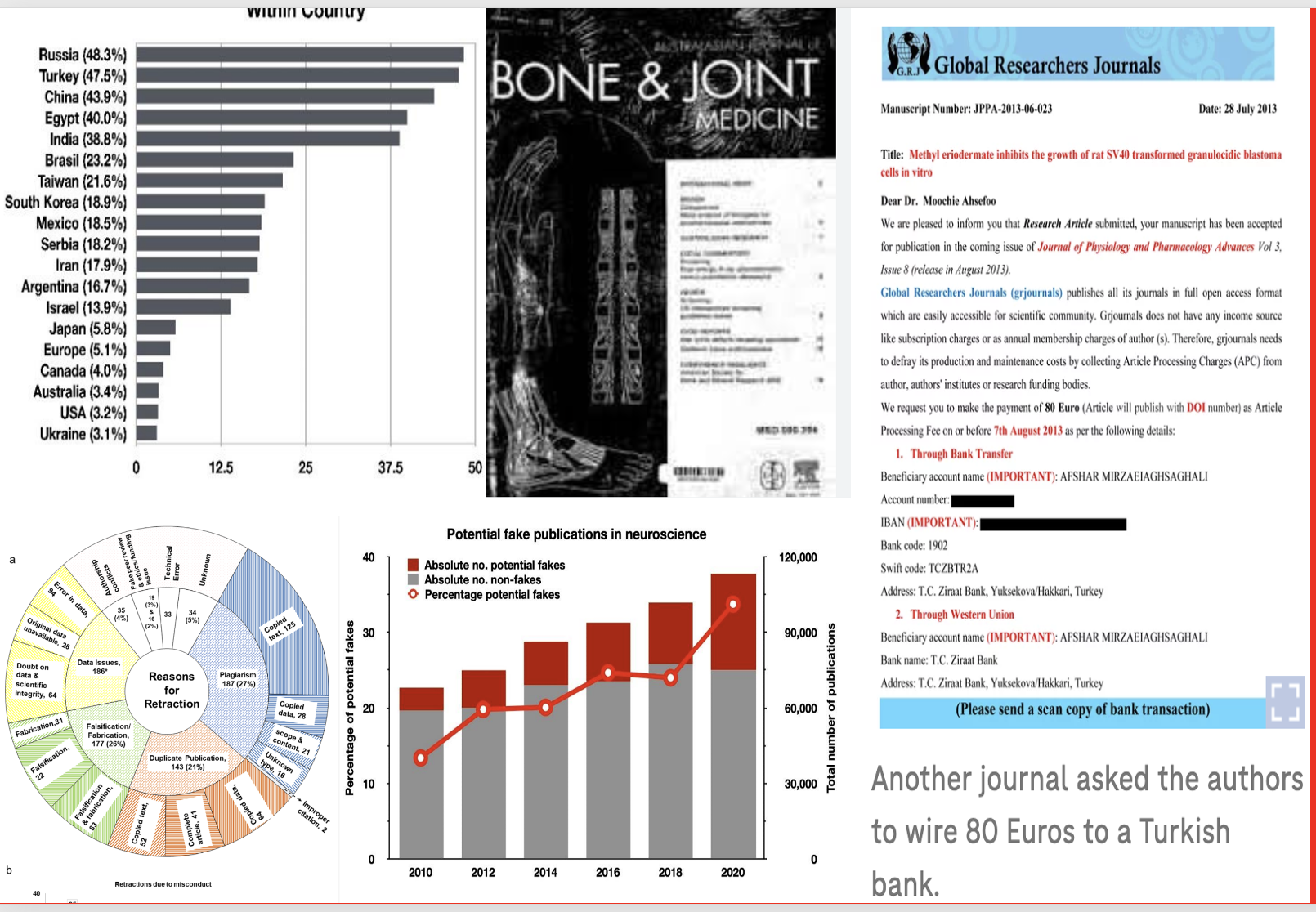
Bir taraftan ilaç sanayii tarafından ticari amaçla üretilen üretilen, diğer taraftan kariyer ilerlemesi-akademik şöhret amacı ile yapılan sahte araştırma yayınların kitlesel olarak üretilmesi bilimin dejenerasyonuna yol açmaktadır. Özellikle son yıllarda yapay zeka destekli otomatik üretim yapan şirketler işi daha da kötüleştirmektedir. Sabel BA ve ark. Yaptıkları araştırmada 2010’dan 2020’ye kadar sahte yayınlarda hızlı bir artış olduğunu ortaya koydu. En yüksek sahte araştırma oranına sahip ülkeler Rusya, Türkiye, Çin, Mısır ve Hindistan’dı (oranlar %39-%55 arasında). 2020 Yılında yayınlanan 1.3 milyon biyomedikal yayının yaklaşık 150.000 tanesi sahte idi. Endüstriyel ölçekteki sahte bilimsel yayıncılık muhtemelen tüm zamanların en büyük bilim sahtekârlığıdır. Mali kaynakların israfına, tıbbi ilerlemenin yavaşlamasına ve muhtemelen hayatların tehlikeye atılmasına neden olmaktadır. İlaç sanayii veya ilaç sanayii destekli yayınlarda seçici veri kullanımı cherry picking), özetlerde yanıltıcı yorumlar, görsel intihali ve açıkça veri uydurma, yan etki ve ölümleri saklama gibi örnekler yer alır. Sahte yayınların en büyük kaynağı, çoğunluğu Çin, Hindistan, Rusya, Birleşik Krallık ve ABD’de bulunan 1.000’den fazla “akademik destek” ajansıdır — yani sözde “makale fabrikaları”dır. Bu makale fabrikaları, internet üzerinden yazım ve düzenleme hizmetlerini tanıtarak, Science Citation Index (SCI) kapsamındaki dergilerde sahte makaleler üretmek ve yayımlamak için yüksek ücretler talep ede). Bu hizmetler, yapay zeka (AI) destekli yarı otomatik şekilde üretilmiş uydurma veriler, grafikler, tablolar ve metinlere dayalı makale üretimini içerir. Makaleler daha sonra bilimsel eğitime sahip profesyonel editörler ve hayalet yazarlar tarafından düzenlenir. Yapılan analizde Rusyadan yapılan yayınların %48.3’ü, Türkiyeden yapılan yayınların %47.5’u, Çinden yapılan yayınların %43.9’u, Mısırdan yapılan yayınların %40’ı ve Hindistandan yapılan yayınların %38.8’ı Hindistandan yapılan yayınların %38.8’i şüpheli sahte yayın olarak değerlendirilmiş (15). Bilimsel sahtekarlıkların ulaştığı son boyut ise ‘’SAHTE DERGİLERDİR’’. Dünyanın en büyük yayın eevlerinden birisi olan Elsevier 6 sahte dergi yayınladı. Bunlardan iki tanesi MERCK ilaç şirketine aitti. Merck, pazarlama aracı olarak hizmet edecek, hakemli bir yayının görünümü ve hissiyatına sahip bir şey yaratması için yayıncı Elsevier'e ödeme yaptı. Bunlar Vioxx ve Fosomax reklamı için ‘’Australasian Journal of Bone & Joint Medicine’’ ve ‘’ Australasian Journal of Bone & Joint Medicine’’ idi.
Bu yazı, biyomedikal ve klinik araştırmalarda bilimsel suistimaller ve dolandırıcılık vakalarının kısaca bir incelemesidir. Birincil veri kaynakları arasında yayınlanan klinik deneyler, yasal belgeler, geri çekilen çalışmalar ve akademik makaleler bulunmaktadır. Ayrıca, doğrudan vaka çalışmalarına ek olarak, bilimsel suistimalleri daha geniş bir perspektiften anlamak için sistematik incelemeler ve meta-analizler de gözden geçirilmiştir. Bu yöntem, suistimallerin bilimsel topluluk ve halk sağlığı üzerindeki etkilerini kapsamlı bir şekilde incelememizi sağlamaktadır. Klinik araştırmalarda bilimsel suistimallerin yaygınlığı, daha sıkı düzenleyici denetimler, daha şeffaf raporlama uygulamaları ve hasta refahına yönelik etik bir bağlılık gerektirmektedir. İncelenen vaka çalışmalarında görüldüğü gibi, hem bireysel araştırmacılar hem de büyük farmasötik şirketler, kişisel veya finansal çıkarlar için verileri manipüle etmekte suçludur. Bu sorunları ele almak için daha iyi dolandırıcılık tespit mekanizmaları, araştırma topluluğunda hesap verebilirliğin artırılması ve araştırmacıların etik sorumlulukları hakkında eğitim verilmesi gerekmektedir. Ancak, bu tür bir çaba ile klinik araştırmaların bütünlüğü yeniden sağlanabilir ve tıbbi bilime duyulan güven korunabilir. Türkiyedeki duruma gelince, akademik yükselmeler için yayın sayısı-atıf sayısı kriteri kaldırılmalıdır. Harvard gibi bazı üniversitelerde her akademik kademe yükselmesi için yayın sayısı kaldırtılmış, onun yerine akademisyenlerin belirli konularda durumuna göre 5-15 yayınını takdim etmesi istenmiştir. Bizde is 20 yayını olan bir tıp mensubunun yayınları 20 değişik konuda olmaktadır. İmece usulü yayılara son verilmelidir. Misafir yazarlıktan vaz geçilmektedir. Yayına direct olarak katkısı olmayan hiçbir kimsenin ismi yayınlara konmamalıdır. Etik kurullar laf olsun diye önüne gelene onay vermemeli, çalışmaların metadolojisi ciddi şekilde incelenmelidir. Bilimsel etik ihlalleri, yalnızca araştırmacılar veya akademisyenler tarafından değil; aynı zamanda editörler, hakemler ve yayınevleri gibi yayın sürecinin diğer aktörlerinin ihmali ya da kasıtlı eylemleriyle de ortaya çıkabilmektedir.
SAHTE ARAŞTIRMALAR SONUÇ:
- Klinik araştırma sonuçları saklandı, yanlız pozitif sonuçlar yayınlandı.
- Klinik araştırmaların sonuçları manipüle edildi ve bazı negative sonuçlar pozitif yapıldı.
- Hayalet yazarlar tarafından yazılan sahte makalelerle sağlıkçılar ve hastalar kandırıldılar.
- Satılmış kanaat önderleri firmalar tarafından satın alınarak doktorları kandırıldı.
- Tedavi rehberlerini ilaç firmaları veya onların seçtirdikleri doktorlar tarafından hazırlandı.
- İlaç firmaları tarafından kurulan veya büyük ölçüde desteklenen dernek ve vakıflar kamuoyunu yanılttı ve ilaçların reklamını yaptı.
- Sahte araştırmalarla ruhsat alan ilaçlar yüzünden milyonlarca dolarlık ekonomik kayıp oldu
- Plasebodan farksız olan birçok ilaç yüzünden hastalar Zarar gördü.
- İlaç firmalarının ilaçlarını yazan doktorlara açık veya gizli menfat temin edildi.
- Ruhsatlandırmadan geri ödemeye kadar her kademede gizli oyunlar
- Biyomedikal alanda sahte araştırmaların bazı örnekleri için: https://en.wikipedia.org/wiki/List_of_scientific_misconduct_incidents; https://www.bmj.com/content/379/bmj-2022-071517?utm_source=chatgpt.com
REFERANSLAR
- Umscheid, CA ve ark., "Key concepts of clinical trials: A narrative review". Postgraduate Medicine. 123194–204, 2011
- Moore, T J ve ark., Estimated costs of pivotal trials for novel therapeutic agents approved by the US Food and Drug Administration, 2015-2016". JAMA Internal Medicine. 178 :1451–1457, 2018
- Vedula SS ve ark., Differences in reporting of analyses in internal company documents versus published trial reports: comparisons in industry-sponsored trials in off-label uses of Gabapentin. PLOS Medicine., 2013, doi:10.1371/journal.pmed.1001378
- Ioannidis JPA, The mass production of redundant, misleading, and conflicted systematic reviews and meta-analyses, L Milbark Quarterly, 94: 485-514, 2016
- Mayor S, Researchhers claim clinical trials are reported with misleading statistics, BMJ, 324: 1353, 2002
- Selective Publication of Antidepressant Trials and Its Influence on Apparent Efficacy. Turner AE, , N Engl J Med 2008; 358:252-260, 2008;
- Tulunay FC, http://www.klinikfarmakoloji.com/index.php/bilimsel-yazilar/olmek-mi-oldurmek-mi-istiyorsunuz-iste-ilaciniz)
- Carlisle JB, False individual patient data and ie randomized controlled trials submitted to Anaesthesia, 76: 444-447, 2022
- ‘hhttp://www.klinikfarmakoloji.com/index.php/editorden/farmakoterapi-kanita-mi-yoksa-sahtekarliga-mi-dayali’’
- Koçyiğit BF ve Akyol A, Analysis of Retracted Publications in The Biomedical Literature from Turkey, J Korean Med Sci, 37: 142, 2022
- Amet F ve ark., Postmortem of Retracted Scientific Publications from Türkiye, Med Res Rep 2023;6: 137-152, 2023
- https://retractionwatch.com/2024/01/09/studies-claiming-islamic-practices-protect-against-disease-and-sexual-harassment-retracted/#more-128535
- https://link.springer.com/article/10.1007/s10096-023-04727-1
- Devine EG., ve ark., Frequency of concealment, fabrication and falsification of study data by deceptive sbjects, Contem.Clin.Trial Comm., 21: 100713, 2021
- Sabell BA ve ark., Fake Publications in Biomedical Science: Red-flagging Method Indicates Mass Production, medRxiv doi.org/10.1101/2023.05.06.23289563; 2023







